谢振华
摘要
以Fe3O4磁性纳米颗粒(MNP,Magnetic Nanoparticles)为基础的纳米复合材料由于其融合了改性剂纳米Fe3O4的优越性能和不同基体材料的特殊优势,有着极为广泛的应用。本文使用化学共沉淀法制备Fe3O4 MNP,并将其与聚乙烯吡咯烷酮(PVP)进行组装,制成Fe3O4 MNP-PVP纳米超顺磁性复合材料。在此基础上以芬顿反应为基本原理,将Fe3O4 MNP-PVP与特定浓度过氧化氢混合制成芬顿试剂,检测抑菌效果和杀菌效果,并表征杀菌原理。
关键词:Fe3O4磁性纳米颗粒、聚乙烯吡咯烷酮、纳米复合材料、芬顿反应、抗菌性能
一、引言
本文采用Fe3O4 MNP-PVP纳米超顺磁性复合材料作为芬顿反应Fe2+源,持续释放Fe2+与H2O2反应生成·OH抗菌。据Wyszogrodzka等人的研究,纳米复合材料本身可作为金属离子储存器,持续缓慢释放金属离子至溶液中[1]。采用考马斯亮蓝G250为显色剂。羟基自由基会进攻考马斯亮蓝G250中具有高电子云密度的-C=C-基团,发生亲电加成反应,使得考马斯亮蓝G250褪色。反应方程式如下:
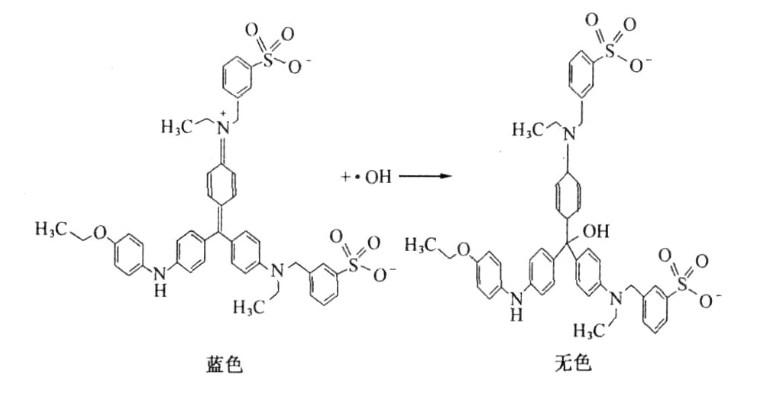
考马斯亮蓝G250的最大吸收波长为582 nm。通过测定检测体系在该波长吸光度的变化,可间接测定羟基自由基的浓度[2]。
二、材料和方法
2.1 实验材料
2.1.1 药品和试剂
二氯化铁·四水(氯化亚铁)、三氯化铁·六水(氯化高铁)、氨水(氢氧化铵)、无水乙醇、聚乙烯吡咯烷酮K16-18[PVP(MW=8000)]、30%过氧化氢、硫酸、高锰酸钾、草酸钠、去离子水、LB肉汤培养基、琼脂
2.1.2 实验菌株
金黄色葡萄球菌(Staphylococcus aureus),本室保存。
2.3 实验步骤与方法
2.3.1 Fe3O4磁性纳米颗粒制备
采用铁盐化学共沉淀法制备,记为Fe3O4 MNP。
2.3.2 Fe3O4磁性纳米颗粒-聚乙烯吡咯烷酮纳米复合材料制备
采用机械搅拌法制备,记为Fe3O4 MNP-PVP。
2.3.3 Fe3O4 MNP-PVP-H2O2体系抗菌性能表征
2.3.3.1 H2O2组分抑菌预备实验
按下表配制LB培养基,绘制金黄色葡萄球菌生长曲线。
表2.4.3.1溶液配比
编号 | H2O2浓度 | 金黄色葡萄球菌浓度 |
1 | 1mol/L | 1x106CFU/mL |
2 | 100mmol/L | |
3 | 10mmol/L | |
4 | 1mmol/L | |
5 | 0.1mmol/L | |
6 | 0.01mmol/L | |
7 | 0mmol/L |
2.3.3.2 Fe3O4 MNP-PVP组分抑菌预备实验
按下表用Fe3O4 MNP-PVP配制LB培养基,绘制金黄色葡萄球菌生长曲线。
表2.3.3.2溶液配比
编号 | Fe3O4浓度 | 金黄色葡萄球菌浓度 |
1 | 1mmol/L | 1x106CFU/mL |
2 | 0.1mmol/L | |
3 | 0.01mmol/L | |
4 | 0mmol/L |
2.3.3.3 Fe3O4 MNP-PVP-H2O2体系抑菌实验
按下表用Fe3O4 MNP-PVP与H2O2配制LB培养基并探究该体系的抑菌作用。
表2.3.3.3溶液配比
编号 | Fe3O4浓度 | 金黄色葡萄球菌浓度 | H2O2浓度 |
1 | 0.1mmol/L | 1x106CFU/mL | 0.1 mmol/L |
2 | 0.08mmol/L | ||
3 | 0.06mmol/L | ||
4 | 0.04mmol/L | ||
5 | 0.02mmol/L | ||
6 | 0mmol/L |
2.3.3.4 Fe3O4 MNP-PVP-H2O2体系杀菌实验
按下表用Fe3O4 MNP-PVP与H2O2配制LB培养基并探究该体系的抑菌作用。
表2.3.3.4溶液配比
编号 | Fe3O4浓度 | 金黄色葡萄球菌浓度 | H2O2浓度 |
1 | 0.1mmol/L | 1x108CFU/mL | 0.1 mmol/L |
2 | 0.08mmol/L | ||
3 | 0.06mmol/L | ||
4 | 0.04mmol/L | ||
5 | 0.02mmol/L | ||
6 | 0mmol/L |
2.3.4 检测H2O2、Fe3O4 MNP-H2O2体系、PVP-H2O2体系、Fe3O4 MNP-PVP-H2O2体系中羟基自由基的产生
按照表2.3.4按从左到右的顺序依次加入试剂配制检测体系,采用考马斯亮蓝分光光度法[2]检测体系中羟基自由基产生的浓度。
表2.3.4溶液配比
编号 | 考马斯亮蓝G250 | 硫酸 | H2O2 | Fe3O4浓度 (Fe3O4 MNP) | PVP浓度 | Fe3O4浓度(Fe3O4 MNP-PVP) |
1 | 0.055g/L 2.5mL | 0.1mol/L 2.0mL | 0.12% 0.6mL | —— | —— | —— |
2 | 0.1mmol/L | —— | —— | |||
3 | —— | 0.1mmol/L | —— | |||
4 | —— | —— | 0.1mmol/L | |||
5 | —— | —— | —— | —— |
三、结果与讨论
3.1 Fe3O4 MNP-PVP-H2O2体系抗菌性能实验结果
3.1.1 单组分预备实验抗菌性能实验结果

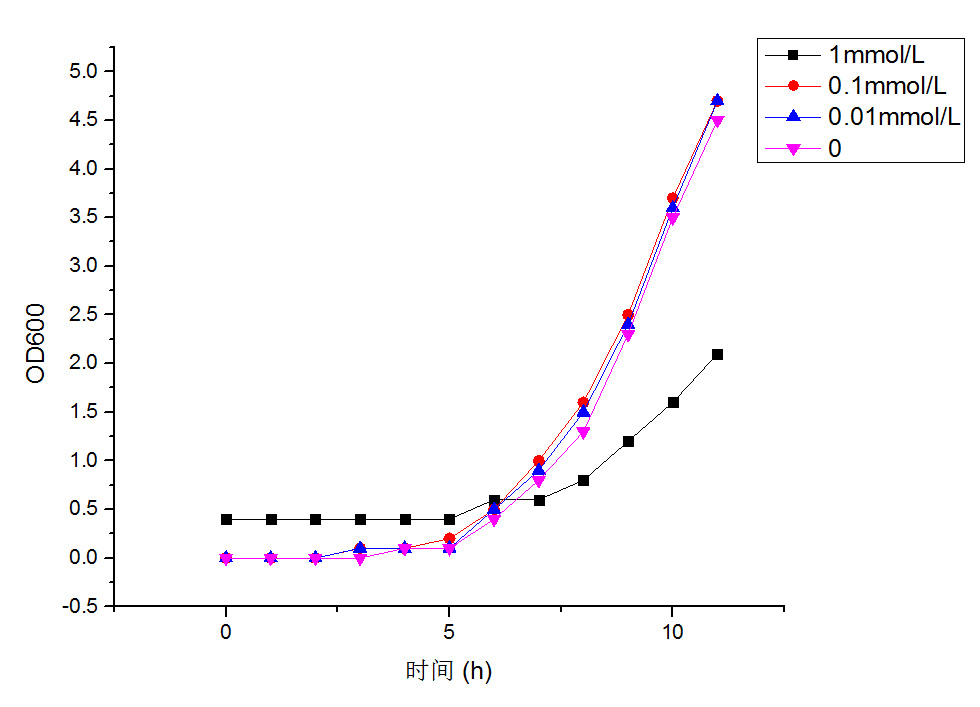
图3.1.1.1 H2O2浓度变化对金黄色葡萄球菌生长的抑制作用(左)
图3.1.1.2 Fe3O4 MNP-PVP浓度变化对金黄色葡萄球菌生长的抑制作用(右)
图3.1.1.1、图3.1.1.2中,可知H2O2浓度<0.1mmol/L、Fe3O4 MNP-PVP浓度<1mmol/L时对金黄色葡萄球菌无抑制作用。因此本实验研究抗菌性能采用的Fe3O4 MNP-PVP-H2O2三元体系各组分浓度范围内任何单一组分均无抑菌作用。
3.1.2 Fe3O4 MNP-PVP-H2O2体系抑菌性能实验结果
为了简化实验流程,本文在研究Fe3O4 MNP-PVP-H2O2体系抑菌性能时,控制H2O2浓度为0.1mmol/L不变,据预备实验可知,此浓度下单独的H2O2无抑菌效果;改变Fe3O4 MNP-PVP浓度,探究体系对金黄色葡萄球菌生长的抑制作用,绘制金黄色葡萄球菌的生长曲线,如图3.1.2所示:
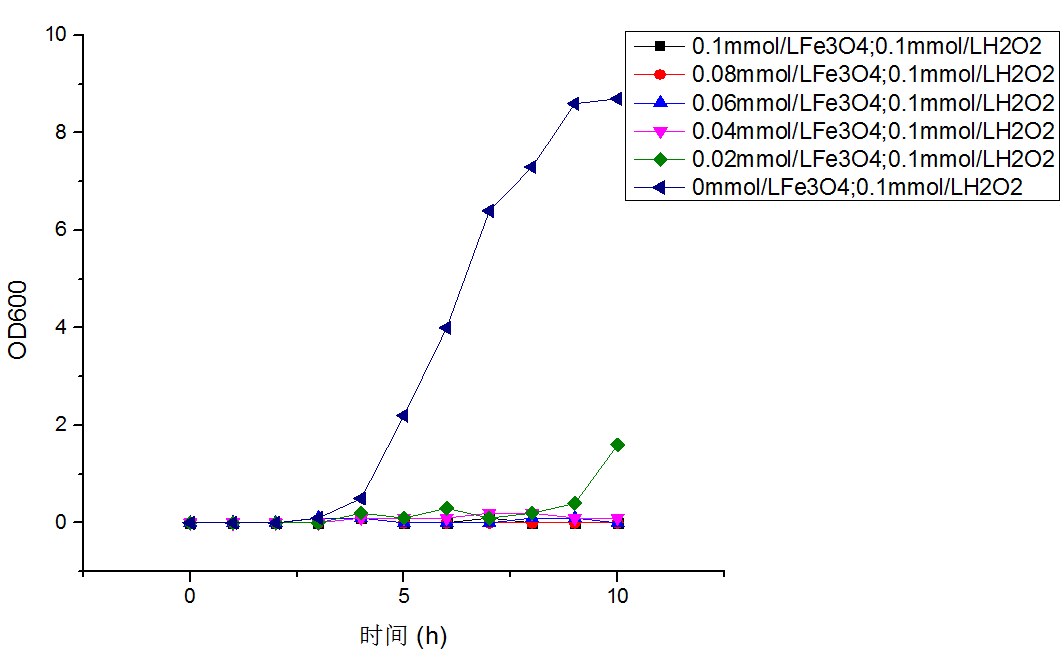
图3.1.2 Fe3O4 MNP-PVP-H2O2浓度变化对金黄色葡萄球菌生长的抑制作用
图3.1.2中,可知即便0.1mmol/L H2O2本身无抑菌效果,但在体系中加入Fe3O4 MNP-PVP后抑菌效果提升,且在一定范围内,加入越多Fe3O4 MNP-PVP抑菌效果提升越显著,说明Fe3O4 MNP-PVP-H2O2体系比任何单一组分抑菌效果更强。
3.1.3 Fe3O4 MNP-PVP-H2O2体系杀菌性能实验结果
在抑菌实验的基础上,利用活细胞计数法研究Fe3O4 MNP-PVP-H2O2体系杀菌性能。同样控制H2O2浓度为0.1mmol/L不变,改变Fe3O4 MNP-PVP浓度,探究体系对1x108CFU/mL金黄色葡萄球菌的杀灭作用。统计一定时间后的存活菌落数(CFU)如表3.1.3:
表3.1.3 Fe3O4 MNP-PVP-H2O2浓度变化对金黄色葡萄球菌生长的杀菌作用
编号 | Fe3O4浓度 | H2O2浓度 | 时间(min) | |||
0 | 10 | 20 | 30 | |||
1 | 0.1mmol/L | 0.1 mmol/L | +++ | + | - | - |
2 | 0.08mmol/L | +++ | + | - | - | |
3 | 0.06mmol/L | +++ | + | + | + | |
4 | 0.04mmol/L | +++ | + | + | + | |
5 | 0.02mmol/L | +++ | +++ | +++ | +++ | |
6 | 0mmol/L | +++ | +++ | +++ | +++ | |
注:+++:细菌存活率>90%;+:细菌存活率<1%;-:细菌存活率= 0或<100/00。
表3.2.3中,可知在一定范围内,加入越多Fe3O4 MNP-PVP体系杀菌效果越显著。
3.2 考马斯亮蓝G250褪色分光光度法检测H2O2、Fe3O4 MNP-H2O2体系、PVP-H2O2体系、Fe3O4 MNP-PVP-H2O2体系中羟基自由基实验结果
实验结果如表3.2所示:
表3.2 考马斯亮蓝G250褪色程度(OD582)
体系 | H2O2 | Fe3O4 MNP-H2O2 | PVP-H2O2 | Fe3O4 MNP-PVP-H2O2 | 空白对照 |
OD582 | 0.484 | 0.421 | 0.488 | 0.420 | 0.493 |
表3.2中,可知H2O2、PVP-H2O2体系考马斯亮蓝G250均未发生褪色现象(或褪色现象不明显),因此体系中均不产生羟基自由基。而Fe3O4 MNP-H2O2、Fe3O4 MNP-PVP-H2O2体系考马斯亮蓝G250发生褪色现象,说明二者中均产生羟基自由基;并且在反应过程中观察颜色变化,即便保证二者中Fe3O4浓度相等,前者褪色速度也比后者要快,但反应完全后褪色程度相差不大,说明前者羟基自由基产生速度较快。
通过整个实验结果可以初步得出结论:Fe3O4 MNP-PVP-H2O2体系能较快速地产生羟基自由基,且主要反应物为Fe3O4 MNP与H2O2,体系中PVP虽不直接参与反应,但其存在减缓了Fe3O4 MNP与H2O2的反应,进而减缓了羟基自由基的生成。
3.3 讨论
3.3.1 Fe3O4 MNP-PVP-H2O2体系的抑菌和杀菌机制
依据考马斯亮蓝G250褪色分光光度法检测羟基自由基的实验结果,可以推断Fe3O4 MNP-PVP-H2O2体系中产生了羟基自由基,因此推测羟基自由基是 Fe3O4 MNP-PVP-H2O2体系的主要杀菌力。体系中各个组分单独拿出来并无很好的抗菌效果,而混合在一起后,Fe3O4 MNP与H2O2发生芬顿反应生成羟基自由基对金黄色葡萄球菌产生抑制或杀灭效果。羟基自由基能作用于微生物细胞的膜系统,改变细胞膜的通透性,使微生物肿胀变形;还能能氧化微生物中的蛋白质和酶分子中的巯基基团,使蛋白质变性,酶的活性和代谢功能丧失,影响微生物正常的新陈代谢功能;还能氧化核酸,破坏 DNA 和 RNA 等,影响微生物基因和其正常表达。这些机制共同作用最终导致微生物生长抑制或死亡[3~7]。
3.3.2 Fe3O4 MNP-PVP-H2O2是一种比H2O2更强的杀菌体系
相对于H2O2,Fe3O4 MNP-PVP-H2O2是一种更强的杀菌体系,其杀菌力源于其芬顿反应产生的羟基自由基。Fe3O4 MNP-PVP-H2O2体系中的H2O2浓度仅为0.1 mmol/L,预备实验可知此浓度下单独的H2O2没有任何抑菌或杀菌活性。因此,相对于H2O2,Fe3O4 MNP-PVP-H2O2是一种强杀菌体系。
3.3.3 Fe3O4 MNP-PVP-H2O2体系应用前景展望
本文试验结果显示,Fe3O4 MNP-PVP-H2O2是一种比H2O2更强的强杀菌体系,在实验条件下对金黄色葡萄球菌有着高效的抑菌、杀菌作用;同时作为主要效应物的羟基自由基具备广谱抗菌作用,因此细菌对Fe3O4 MNP-PVP-H2O2体系不产生抗性突变;有机配体PVP独特的性质改良了Fe3O4 MNP,令体系更为稳定、分散,也具有更好的生物相容性以及PVP本身的其它作用。这显示Fe3O4 MNP-PVP-H2O2杀菌体系在治疗表面创伤或其它局部感染的用药方面,以及污水处理等方面,都有极大应用价值。Fe3O4 MNP-PVP-H2O2作为一种强杀菌体系,其强杀菌能力有目共睹。其组分安全无毒、来源广泛、制备简单、使用方便,并且可以根据实际需求改变组分类型及配比,有着广泛的适用性。
四、参考文献
[1]Wyszogrodzka Gabriela, Marszałek Bartosz, Gil Barbara,etc.Metal-organic frameworks: mechanisms of antibacterial action and potential applications.[J].Drug discovery today,2016,Vol.21(6):1009-1018.
[2]刘瑛,陈新,薛翠华.考马斯亮蓝G250褪色光度法测定Fenton反应产生的羟基自由基[J].理化检验(化学分册),2010,46(05):475-477+481.
[3]孟甄,金建玲,高培基.细菌耐药性的诱导与消除.中国药理学通报(Chinese pharmacological bulletin),2003,19(9) :1047-1051.
[4]Hippeli,S. & Elstner,E. F. OHradicaltype reactive oxygen species: a short review on the mechanisms of OHradical and peroxynitrite toxicity. Zeitschrift für Naturforschung. C,Journal of biosciences,1997,52c:555-563.
[5]Spiegeller P,Sermon J,Vanoirbeek K,Aertsen A,Wichiels C. Role of porins in sensitivity of Escherichia coli to antibacterial activity of the lactoperoxidase enzyme system. Applied and environmental microbiology,2005,71(7) :3512-3518.
[6]Wright C,Bowie J,Gary G,Nelson R. Candidacidal activity of myeloperoxidse: Mechanisms of inhibitory influence of soluble cell wall mannan. Infection and immunology,1983,42(1) :76-80.
[7]Thomas E, Aune T. Oxidation of Escherichia coli sulfhydryl components by the peroxidase-hydrogen peroxideIodide antimicrobial system. Antimicrobial agents and chemotherapy,1978,13(6) :1006-1010.

地址:岳阳市经济技术开发区康王乡新华社区-岳阳市弘毅新华中学(京港澳高速路连接线3公里处、南翔万商旁)
联系电话:0730-8061333
Copyright © 2010-2017 岳阳市弘毅新华中学 湘ICP备18022682号 技术支持:连线科技

官方二维码